16 октября 2020
Что такое генетика?
Генетика определяет многие признаки нашего организма. Эта информация зашифрована в ДНК. Последовательность ДНК идентична во всех клетках организма, кроме половых, и может претерпевать лишь незначительные изменения с возрастом (соматические мутации). Последовательность ДНК является матрицей, которая определяет строение всех белков нашего организма, а также то, сколько этих белков будет нарабатываться. Иными словами, практически все функции и биохимические процессы зависят от ДНК.Однако не только ДНК определяет признаки нашего организма. В исследованиях на близнецах было показано, что даже при полной идентичности генома близнецы могли отличаться множеством признаков. Ученые продолжительное время исследовали этот вопрос и выяснили, что помимо генетики есть еще множество факторов, влияющих на активность наших генов. Их назвали «эпигенетические факторы».
Существует несколько уровней эпигенетической регуляции. Первый – химические модификации самой ДНК (наиболее распространенное – метилирование) или окружающих ее белков (хроматина). Все эти модификации определяют, насколько ДНК будет доступна для взаимодействия. С помощью других механизмов (РНК-интерференция) регулируется скорость образования белковых молекул (трансляция). С помощью эпигенетики также регулируется скорость созревания белковых молекул (фолдинг белков). Иными словами, эпигенетические механизмы определяют, насколько активны будут те или иные гены и белки.
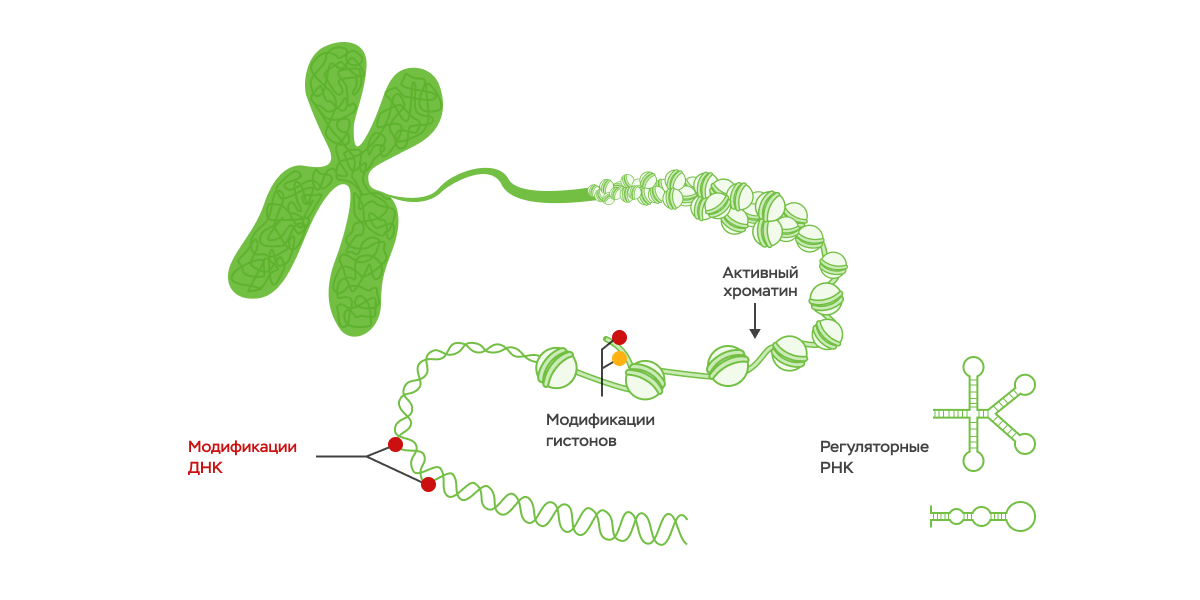
Механизмы эпигенетической регуляции – это эволюционное приобретение, поскольку они позволяют хорошо адаптироваться к изменяющимся условиям окружающей среды. Множество исследований как на животных моделях, так и на человеке позволили установить, что распределение эпигенетических модификаций в геноме изменяется в ответ на пережитый стресс, прием различных фармпрепаратов и лекарственных средств, гормональную терапию, изменения в условиях окружающей среды и др.
Важную роль здесь играют сила воздействия фактора и его длительность. Наиболее негативные эффекты связаны с хроническими воздействиями, например, продолжительный стресс способен привести к развитию депрессии. Но даже кратковременный опыт сильного стресса (травма, сильное эмоциональное потрясение) также может стать причиной развития посттравматического расстройства. Также эпигенетические изменения влияют на обмен веществ. Например, в исследованиях было доказано, что дети, получающие недостаточно питания в детстве, имеют повышенный риск развития диабета 2-го типа во взрослом возрасте [1].

Тем не менее не все люди одинаково реагируют на изменения окружающей среды. Вы, наверное, обращали внимание, что одни легко переносят любые невзгоды, в то время как даже незначительные трудности для других становятся настоящим испытанием и способствуют развитию депрессивноподобного состояния. «За все это отвечает эпигенетика?» – спросите вы. Ответ на этот вопрос заключается в том, что генетика и эпигенетика тесно связаны друг с другом, существует даже понятие «ген-средовое взаимодействие».
Эта концепция предполагает, что в зависимости от индивидуальных генетических особенностей люди могут по-разному реагировать на изменяющиеся условия внешней среды. В пилотной работе еще в 2003 году доктор Каспи показал, что у носителей короткой формы гена транспортера серотонина 5-HTTLPR (S-аллель) депрессия развивается чаще, если у них был стресс в детстве [2]. Схожая ситуация наблюдается и у носителей аллеля риска гена MAOA, белковый продукт которого отвечает за расщепление нейромедиаторов. Носители негативного аллеля, подвергнутые стрессу, в детстве чаще проявляют антисоциальное поведение [3].
Эти поведенческие особенности, по всей видимости, связаны с нарушением сигналинга моноаминовых нейромедиаторов, который зависит как от генетической, так и от средовой компоненты. Синтез этих нейромедиаторов, таких как серотонин, норадреналин и дофамин, происходит в мозгу из предшественников, поступающих к нам из пищи. Поэтому вклад «плохой генетики» можно снизить правильным питанием и изменением образа жизни. А какой генотип генов 5-HTTLPR и MAOA у вас? Как снизить уровень стресса, апатии и депрессии? Ответы на все эти вопросы можно найти в тесте MyNeuro.

Интересно, что существуют две основные теории чувствительности/устойчивости к негативным условиям внешней среды. Одна из них предполагает, что изначально есть люди с «хорошей» и «плохой» генетикой, которая определяет их чувствительность к стрессу и другим негативным факторам. Другая теория – «дифференциальной чувствительности» предполагает, что люди отличаются друг от друга по выраженности их ответов на различные факторы, как позитивные, так и негативные. Другими словами, при воздействии негативных факторов люди с повышенной чувствительностью более склонны к негативным проявлениям, в то же время в хороших условиях у них быстрее проявляются позитивные изменения.
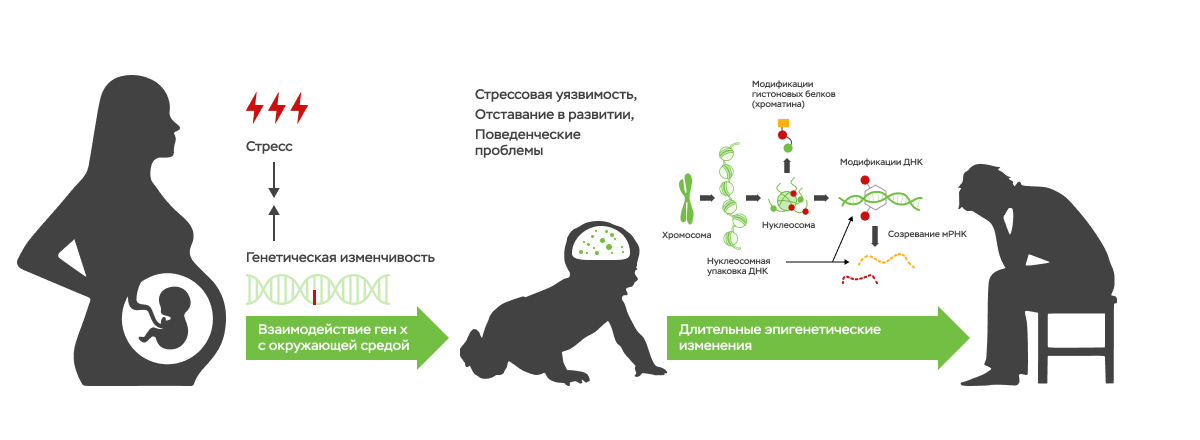
Окружающая среда воздействует на наши гены на всех этапах индивидуального развития. Хорошо известно влияние внутриутробного развития на метаболизм во взрослом возрасте. Недостаточное потребление калорий во время беременности в период голода во Вторую мировую войну, так же как и во время других войн, приводило к рождению детей с низким весом. У них чаще, чем у других, наблюдались метаболические (сахарный диабет и др.) и сердечно-сосудистые заболевания во взрослом возрасте [4]. Механизм подобных эффектов, по всей видимости, связан с тем, что эмбрион адаптируется к недостаточному и нерегулярному потреблению нутриентов с помощью выстраивания эпигенетической программы «сохранить как можно больше». Другими словами, он пытается максимально использовать недостаточный ресурс, что в условиях нормального количества нутриентов приводит к метаболическим расстройствам.
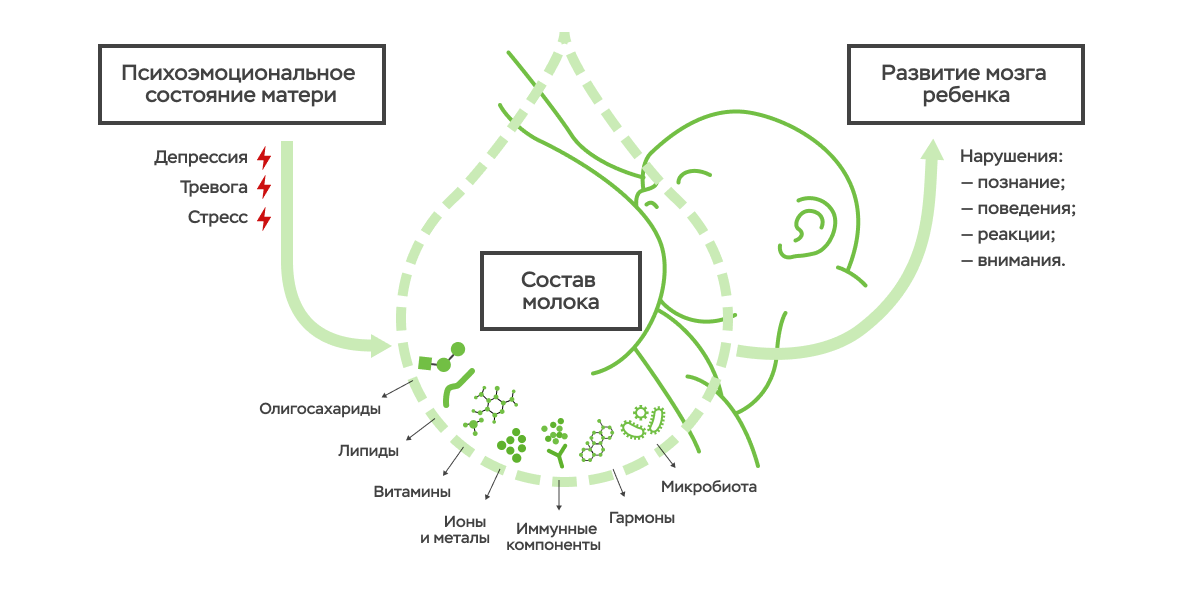
Влияние среды опосредуется и в младенчестве. Например, психоэмоциональное состояние и питание матери напрямую определяют состав ее молока, что, в свою очередь, влияет на особенности развития ребенка. Более того, даже те события, которые произошли до зачатия, способны оставить след на потомстве, поскольку могут привести к эпигенетическим изменениям в гормональной регуляции матери. Таким образом, можно сказать, что здесь наблюдается так называемое эпигенетическое наследование, когда предыдущий опыт родителей, бабушек и дедушек откладывает отпечаток на потомстве.
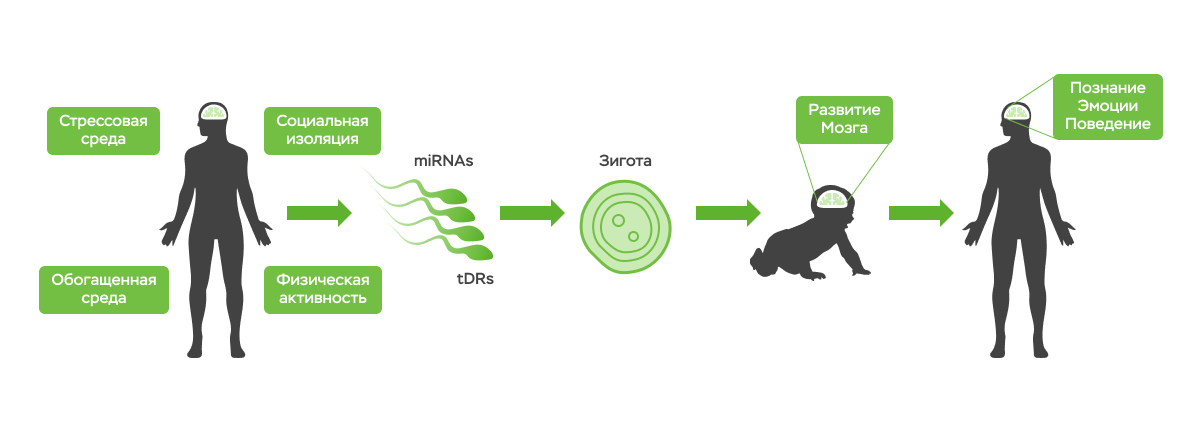
Молекулярный механизм такого наследования до конца не ясен. Однако работы на животных показывают, что эффекты стресса способны «передаваться» в 3–4 поколениях благодаря эпигенетике [5]. Интересно, что доказательства эпигенетического наследования также найдены и в работах на людях [6]. Например, дочери, чьи матери во время своего внутриутробного периода развития получали недостаточное количество питательных веществ (описанные выше), имели в 1,8 раза чаще метаболические заболевания [7], а их внуки имели более высокий индекс массы тела, чем в среднем по популяции [8]. Так что помните, никакие события в нашей жизни и жизни наших предков не проходят бесследно для нашего организма, каждое из них оставляет свой «эпигенетический след».
Автор: Василий Решетников, нейробиолог, разработчик Национального центра генетических исследований
Источники:
- Wang N., Wang X., Han B. et al. Is exposure to famine in childhood and economic development in adulthood associated with diabetes? // The Journal of Clinical Endocrinology & Metabolism. – 2015. – Vol. 100. – No. 12. – P. 4514–4523.
- Caspi A., Sugden K., Moffitt T. E. et al. Influence of life stress on depression: moderation by a polymorphism in the 5-HTT gene // Science. – 2003. – Vol. 301. – No. 5631. – P. 386–389.
- Caspi A., McClay J., Moffitt T. E. et al. Role of genotype in the cycle of violence in maltreated children // Science. – 2002. – Vol. 297. – No. 5582. – P. 851–854.
- Vaiserman A. M. Early-life nutritional programming of type 2 diabetes: experimental and quasi-experimental evidence // Nutrients. – 2017. – Vol. 9. – No. 3. – P. 236.
- van Steenwyk G., Roszkowski M., Manuella F. et al. Transgenerational inheritance of behavioral and metabolic effects of paternal exposure to traumatic stress in early postnatal life: evidence in the 4th generation // Environmental epigenetics. – 2018. – Vol. 4. – No. 2. – dvy023.
- King S. E., Skinner M. K. Epigenetic Transgenerational Inheritance of Obesity Susceptibility // Trends Endocrinol Metab. – 2020. – Vol. 31. – No. 7. – P. 478–494.
- Painter R. C., Osmond C., Gluckman P. et al. Transgenerational effects of prenatal exposure to the Dutch famine on neonatal adiposity and health in later life // BJOG: An International Journal of Obstetrics & Gynaecology. – 2008. – Vol. 115. – No. 10. – P. 1243–1249.
- Veenendaal M. V., Painter R. C., de Rooij S. R. et al. Transgenerational effects of prenatal exposure to the 1944–45 Dutch famine // BJOG: An International Journal of Obstetrics & Gynaecology. – 2013. – Vol. 120. – No. 5. – P. 548–554.
Подробнее о ДНК тестах
Смотрите также
Предыдущая
Следующая






